Evaluación de la movilidad del boro en un hierro puro ARMCO endurecido a través del proceso borurización base polvo
Resumen
En el presente estudio se evalúa la cinética de difusión del boro en el hierro puro ARMCO® durante el proceso de borurización base polvo. Esta técnica de endurecimiento superficial produce en el material la formación de una base característica, Fe2B. El tratamiento termoquímico se realizó a las temperaturas de 1123, 1173, 1223 y 1273 K con tiempos de 2, 4, 6 y 8 h. Empleando la ecuación de balance de masa en la interface de crecimiento Fe2B/substrato (AC(dx/dt)x=v=2sD1/2t1/2=Jin(x)x=v-Jout(x)x=v+dv) y sin la consideración de un perfil de concentración de boro a lo largo de la fase Fe2B, se determinó la movilidad del boro en la superficie del substrato (DFe2B), con la influencia del tiempo de incubación (t0Fe2B). Para validar el modelo de difusión propuesto, el valor simulado para el espesor de capa Fe2B se comparado con el valor experimental obtenido para temperatura de tratamiento de 1253 K y para un tiempo de 5 h. La morfología de la capa Fe2B fue observada a través de Microscopía Electrónica de Barrido (SEM) y Microscopía Óptica. Los estudios metalográficos mostraron que la capa borurada presenta un morfología aserrada en la interface de crecimiento para todas las muestras endurecidas. Los espesores de las capas fueron medidos con ayuda del software MSQ PLUS. La fase Fe2B fue identificada a través de la técnica difracción de rayos X (XRD). Finalmente, la adherencia de las capas Fe2B sobre la superficie del substrato fue evaluada con ayuda de la técnica de indentación Daimler-Benz Rockwell-C. Asimismo, el valor estimado de la energía de activación del boro fue comparado con la literatura.
Palabras clave: Energía de activación, Adherencia, Borurización, Modelo de difusión, Cinética de crecimiento
Abstract
In this study, the growth kinetics of boron on ARMCO® iron substrate by powder-pack boriding process was carried out. This superficial hardening technique produce the formation of a single-phase (Fe2B). Thermochemical treatment for ARMCO® iron was made in the temperature range of 1123-1273 K for treatment times ranging from 2 to 8 h. The boron diffusion coefficient in the Fe2B layers was estimated by solving the mass balance equation (AC(dx/dt)x=v=2sD1/2t1/2=Jin(x)x=v-Jout(x)x=v+dv) at the (Fe2B/substrate) interface with an inclusion of boride incubation time. To validate the present model, the simulated value of Fe2B layer thickness was compared with the experimental value obtained at 1253 K for a treatment time of 5 h. The morphology of Fe2B layers was observed by SEM and optical microscopy. Metallographic studies showed that the boride layer has a saw-tooth morphology in all the samples. The layer thickness measurements were done with the help of MSQ PLUS software. The Fe2B phase was identified by X-ray diffraction method. Finally, the adherence of Fe2B layers on the ARMCO® iron substrate was qualitatively evaluated by using the Daimler-Benz Rockwell-C indentation technique. In addition, the estimated value or boron activation energy was compared to the literature data.
Keywords: Activation energy, Adherence, Boriding, Diffusion model, Growth kinetic.
1. Introducción
La borurización es un tratamiento termoquímico empleado para el endurecimiento de superficies de aleaciones ferrosas y no ferrosas [1]. En el tratamiento de borurización, los átomos de boro debido a su tamaño es más pequeño en comparación con los átomos de hierro [2] se difunden con relativa facilidad en la superficie de la pieza para formar boruros de hierro en el rango de temperatura de 973-1323 K [1-2. Después de aplicar el proceso de borurización, la capa formada en la medios sólidos.
Dependiendo de la temperatura del proceso, la composición superficie del acero incrementa la dureza superficial, disminuye el desgaste y la corrosión [2-15]. El proceso de borurización se puede realizar en forma líquida, gaseosa o en química del sustrato, el potencial del medio borurante y tiempo de tratamiento, es posible formar una monocapa (Fe2B) o una bicapa (FeB + Fe2B) [16, 17]. La fase FeB con una estructura cristalina ortorrómbica con un contenido de boro de 100.5 x103 mol m-3, mientras que la fase Fe2B tiene una estructura cristalina tetragonal centrada en el cuerpo con un contenido de boro de 59.2x103 mol m-3 [18-20]. La formación de una doble capa (FeB + Fe2B) se puede obtener ajustando el potencial químico del boro en el medio borurante [21].
El crecimiento y morfología de las fases boruradas puede verse afectada por los elementos de aleación en el material base [22-24]. Frentes de crecimiento con morfología aserrada de la capa borurada aparece en el hierro puro y aceros de baja aleación. La morfología aserrada se debe a la alta anisotropía del coeficiente de difusión en la red cristalina tetragonal de la fase Fe2B. Puesto que la orientación [100] representa la orientación de la red con la máxima velocidad de difusión del átomo de boro, a mayor tiempo de tratamiento, se forma una textura [3] [100] más sólida. Cuando los elementos de aleación y/o el contenido en carbono aumenta, la morfología aserrada desaparece, y para aceros de alta aleación se forma la denominada intercara [1].
Este hecho experimental fue explicado por Carbucicchio et al. [24], donde los átomos sustitucionales de elementos tales como Mo, V, Cr y Ni tienden a concentrarse en las puntas de las columnas del boruro de hierro. Esta concentración de elementos de aleación en las puntas reduce considerablemente el flujo de boro activo en esta zona y en consecuencia, se forma una suave y plana interfase de crecimiento (capa/substrato) [25, 26]. En aplicaciones prácticas, la selección de los parámetros del proceso es muy importante para alcanzar el espesor deseado de capa borurada [27,28]. Una estimación de la cinética de crecimiento de las capas boruradas es una herramienta conveniente para la optimización y automatización del proceso de borurización [29, 30].
Con este fin, diferentes modelos han sido reportados en la literatura para simular la cinética de crecimiento de las capas boruradas en función de los parámetros del proceso pero sin la consideración del periodo de incubación (t0Fe2B) [31-77].En estos modelos se asume que los boruros de hierro crecen de manera instantánea (t=0). En el presente estudio se determina una nueva ecuación que permite estimar los espesores de capa de la fase Fe2B a través de un modelo de difusión de transferencia de masa para la simulación de la cinética de crecimiento de los boruros de hierro formados en la superficie del hierro puro ARMCO®, en el rango de temperaturas de 1123-1273 K empleando la técnica de borurización de polvo [78, 79]. En este modelo de difusión se propone una ecuación de balance de masa en la interfase de crecimiento Fe2B/substrato sin considerar un perfil de concentración de boro a lo largo de la fase borurada.
Asimismo, se asume que los boruros de hierro obedecen la ley de crecimiento parabólico (v=2ED1/2Fe2Bt1/2)para estimar el coeficiente de difusión del boro en la fase Fe2B(DFe2B). Combinando el coeficiente de difusión y la ley de crecimiento parabólico es posible estimar el espesor de capa en la fase Fe2B en función de la temperatura y tiempo de tratamiento.
2. Modelo de difusión
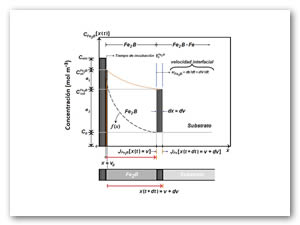
En la propuesta del modelo de difusión, se ha partido de la suposición de que las capas no comienzan a formarse instantáneamente (t=0), sino a partir de un cierto periodo de incubación, (t0Fe2B) en el cual ya se tiene un perfil inicial no nulo f(x(t)) de boro disociado en la capa superficial del metal (ver Figura 1), cuando comienza la formación de capas. A partir del perfil inicial, una capa de boruros de hierro comienza a formarse y se extiende lentamente al interior del substrato. La existencia del instante y del perfil inicial mencionado (f(x(t))) ), son realmente una consecuencia de los procesos de incubación y coalescencia [4] de la fase en la etapa inicial de su gestación [5].
Sin embargo, dado que no se tiene información más detallada sobre la física de estos procesos que permita modelarlos matemáticamente, se ha propuesto un elemento novedoso que permite “imitar el resultado” de los procesos físicos reales, así como determinar teóricamente valores experimentalmente justificados tanto para el instante inicial t0Fe2B como para el perfil inicial de concentración de boro disociado mencionado arriba. Este argumento novedoso, es congruente con la observación experimental de la existencia de un valor umbral de concentración superficial a partir del cual comienzan a generarse las capas de boruros [29].
La consideración física en la cual se sustituyen los complejos procesos subyacentes en la etapa inicial del proceso de borurización, consiste en suponer que, desde el instante inicial t=0 hasta el instante t0Fe2B en que se alcanza el requerido umbral superficial de concentración CupFe2B, formando una pequeña películas base (v0) de unos cuantos nanómetros de espesor (≈5 nm) en la fase Fe2B, ocurre un proceso de transporte de boro en la austenita [6] sobresaturada desde la superficie, mediante un mecanismo de difusión estándar que da lugar al perfil inicial de concentración requerido para que comiencen a distinguirse la fase de boruros (Fe2B). De esta forma, se ha llegado a un modelo de difusión con fronteras libres y con saltos de concentración en las interfases. El modelo se aplica a una situación realista en que se borura una muestra de metal con profundidad finita L.
Cuando L es “pequeño” se impone una condición de flujo nulo en el fondo (x=L) de la muestra o una concentración nula si L se supone “suficientemente grande”. No se asume un perfil de concentración para la fase formada (Fe2B) en la superficie del hierro puro ARMCO®. Lo que se quiere es determinar los coeficientes de difusión (DFe2B)a partir de mediciones de concentración a diferentes profundidades (v)en cada una de las capas, resulta más conveniente utilizar el modelo del estado estacionario debido a su sencillez y también al hecho de que sólo en el estado estacionario es posible asegurar de que las mediciones de la concentración tomadas a una profundidad fija corresponden a una única fase. De tal manera que las condiciones inicial y las de frontera para CFe2B[x(t] son (ver Figura 1):
(1)
(2)
(la concetración superficial se mantiene constante), para
(3)
(la concetración superficial se mantiene constante), para
CupFe2Brepresenta el límite superior de concentración de boro en la capa Fe2B, ClowFe2B es el límite inferior de concentración de boro en la capa Fe2B [26], t representa el tiempo de tratamiento (s), v es la profundidad de la capa (m) y v0 representa una película base en la etapa de nucleación de unos nanómetros de espesor (≈5 nm) [73], la cual puede ser considerada cero (v0≈0) en comparación con el espesor de la capa borurada (v). El término CadsFe2B representa la concentración de boro adsorbido en la superficie del material [26]. Para construir el modelo matemático de crecimiento de capas (Fe2B) se hicieron las siguientes suposiciones:
- (I) Una vez alcanzado el valor umbral de la concentración de boro CupFe2Ben la superficie, comienza la formación de capas en frentes planos.
- (II) Se forma una película base de Fe2B (v0), la cual termina con la aparición de los primeros boruros de hierro después de un cierto tiempo de incubación [7].
- (III) La capa borurada crece como consecuencia de la difusión perpendicular de boro en la superficie del material.
- (IV) La formación de capa Fe2B ocurre bajo condiciones de equilibrio termodinámico.
- (V) No se asume un perfil de concentración de boro a lo largo de la fase Fe2B.
- (VI) La cinética de crecimiento es controlada por la difusión de átomos de boro en la formación de la capa Fe2B.
- (VII) El flujo es unidimensional.
- (VIII) La concentración de boro en la superficie e interfase de crecimiento permanecen constantes en la capa borurada durante el tratamiento.
- (IX) La capa borurada es delgada en comparación al espesor de la muestra.
- (X) La temperatura en cada punto de la muestra es idéntica durante todo el proceso.
- (XI) El medio borurante no varía con el tiempo.
- (XII) Las capas boruradas obedecen la ley de crecimiento parabólico (v=2ED1/2Fe2Bt1/2)
Si el área unitaria de la interfase plana Fe2B/Fe, se mueve una distancia dv en un tiempo dt, (donde representa el tiempo efectivo de formación de la fase) en el volumen (dv*1*1), como se puede apreciar en la Figura 1, es decir, el incremento dv del espesor de capa Fe2B en un tiempo dt ocurre bajo el consumo simultáneo de la capa de espesor dv del substrato. Por lo que, la acumulación de átomos de boro en el incremento dv se puede expresar de la siguiente manera:
(4)
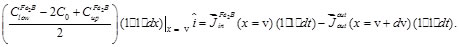
Por otro lado, hay un flujo de átomos de boro hacia la interfase de la fase Fe2B igual a
y un flujo saliente de la interfase en la fase Fe igual a
en un tiempo dt. La Ecuación (4), representa la conservación de la masa. Las concentraciones CupFe2B, ClowFe2B y C0de la Ecuación (4) son expresadas en porcentaje en (mol m3). Con C0≈0,CupFe2B=100.5x103 molm-3. La relación usual entre el flujo y el gradiente de concentración están dados por la primera ley de Fick y si se asume que el perfil de concentración de boro en la fase Fe2B y en el sustrato Fe sólo depende de la posición x(t), por lo que se tiene:
(5)
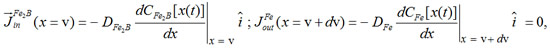
donde DFe2B es el coeficiente de difusión del boro a través de la fase Fe2B y DFe
es el coeficiente de difusión del boro en el substrato. La suposición de que JFeout(x=v+dv)=0 ,tiene que ver con que la solubilidad[8] del boro en la fase Fe (substrato) es muy baja (C0≈0). Combinando las Ecuaciones (5) y (4) se produce lo siguiente:
(6)
Aplicando la regla de la cadena en el lado derecho de la Ecuación (6) resulta en:
(7)
El término dCFe2B[x(t)]/dt, no es cero, de acuerdo con la diferencial total de la función CFe2B[x(t)] es [80]:
(8)
Derivando con respecto a t la Ecuación (9), se tiene:
(9)
De la Ecuación (9), es claro que dCFe2B[x(t)]/dt no es cero. Analizando los términos del lado derecho de la Ecuación (9), la derivada de CFe2B[x(t)] con respecto a x(t) no se anula debido que la concentración es función de la posición. En cuanto al término dx(t)/dt, la posición depende del tiempo desde que se asume que el crecimiento de las capas boruradas obedecen la ley de crecimiento parabólico [26, 30]:
(10)
El término tv en la Ecuación (10) representa el tiempo efectivo de formación de la capa Fe2B y E determina el parámetro de normalización de crecimiento de la fase Fe2B.
(11)
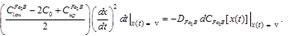
Evaluando el lado izquierdo de la Ecuación (11) con la ecuación (10), integrando ambos lados, correspondiendo ambos límites de integración, obteniéndose lo siguiente:
(12)
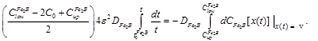
De la Ecuación (12), resulta en:
(13)
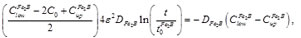
(14)
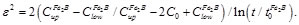
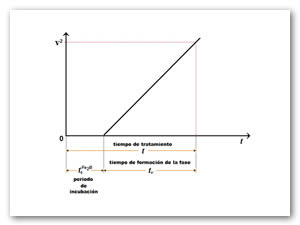
De la Ecuación (14), se debe considerar t > t0Fe2B, para asegurar la formación de la fase Fe2B (ver Figura 2).
3. Procedimiento experimental
Se empleó hierro puro ARMCO® con una composición química que se presenta en la Tabla 1. Las probetas fueron cortadas en un torno de control numérico (CNC) HASS, para eliminar los esfuerzos residuales en las muestras creados por el endurecimiento por deformación, fueron recristalizadas a 923 K. Como consecuencia del corte de las probetas, las superficies tienen un acabado rugoso y generalmente desigual.
Tabla 1. Composición química en wt. % del substrato empleado en el proceso de borurización en pasta.
| Tipo de acero | C | Mn | Si | P | S | Cr | N | Sn | Cu |
| Hierro puro ARMCO® | 0.010 | 0.10 | --- | 0.010 | 0.008 | --- | 0.006 | 0.010 | 0.03 |
Para el tratamiento de borurización en polvo[9] con la técnica de empaquetamiento en caja utilizando carburo de boro (B4C) (Durborid-mezcla de polvo fresco), potasio fluoroborato (KBF4) como activador principal, carburo de silicio (SiC) como principial diluyente y oxigeno del medio circundante en la atmósfera (O2) [77] induciendo la reacción de boro con la superficie del substrato y se emplean contenedores de acero inoxidable AISI 304L grado médico, debido a que son menos propensos al efecto del calor y la descarburización.
Los contenedores se fabrican de acuerdo al tamaño y geometría de la probeta. Otro punto importante a considerar es que si los contenedores son nuevos, se deben tratar previamente con carburo de boro, con la intensión de saturar las paredes. El contenedor se coloca en una mufla convencional a la temperatura de 1273 K y un tiempo de tratamiento de 10 h. Continuando con el proceso de borurización de empaquetamiento en caja. Se introducen las piezas a borurar en el contenedor, en su interior debe contener una mezcla de carburo de boro (Durborid-mezcla de polvo fresco), posteriormente se debe sellar [79]. El esquema de colocación de la probeta se presenta en la Figura 3. La tapa del contenedor debe embonar lo suficiente para no permitir la entrada de oxígeno, ya que puede reaccionar con la composición del medio borurante formando CO y un óxido que obstaculiza el proceso, consumiendo el boro activo en forma de B2O2, y llega a generar porosidades en la superficie del substrato. El alto grado de porosidad en las fases formadas implica un decremento en sus propiedades mecánicas, debido a que presenta puntos de concentración de esfuerzos residuales [80-82].
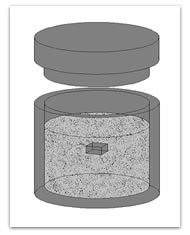
Figura 3. Esquema de colocación de la probeta dentro del contenedor de acero inoxidable 304L con la mezcla de polvos.
Para realizar el proceso de borurización, las probetas se colocaron de nueva cuenta en la mufla, posteriormente se satura la cámara del horno con gas inerte, en este caso se utiliza gas argón de alta pureza (Ar). Es muy importante mencionar que la atmósfera inerte de argón debe mantenerse durante todo el proceso.
Posteriormente se eleva la temperatura previamente establecida en un rango de 1073-1323 K y se inicia el tratamiento hasta alcanzar el tiempo fijado en el diseño experimental. En este punto se abre la mufla para retirar las muestras. Una vez concluido el tratamiento de borurización en polvo, las muestras fueron colocadas en un cuarto a temperatura ambiente. Las probetas fueron cortadas transversalmente, utilizando un disco de diamante serie 15HC con diámetro de 127 mm y un espesor de 0.5 mm; posteriormente, las muestras se encapsularon en bakelita (polvo fenólico) o lucita, con una altura máxima de 25 mm, como lo establece la norma de Preparación Metalográfica de Especímenes ASTM-E3, con esto se asegura el adecuado desbaste de las mismas.
El montaje de las piezas puede ser por medio de una montadora manual o eléctrica. Una vez montadas las muestras, se procede a desbastar la superficie empleando hojas abrasivas de carburo de silicio con una secuencia de grano: 80, 120, 220, 240, 320, 400, 600, 1000, 1500 y 2000 con el objetivo de obtener un acabado superficial de espejo. Este proceso puede realizarse, ya sea manualmente sobre una superficie rígida, lisa y libre de impurezas. El desbaste de las muestras con la lija de carburo de silicio 2000 facilita y disminuye el tiempo de pulido. Se empleó un paño micro-cloth, utilizando como abrasivo alúmina con una granulometría de 0.3 y 0.5 μm y agua destilada como lubricante y disipador de calor, continuando con un pulido con sílice coloidal y alcohol etílico como lubricante, y por último, las muestras se pulen con pasta de diamante sintético con una granulometría de 3 μm y etilenglicol como lubricante empleando. Las muestras se pulen hasta quedar como espejo sin la presencia de rayones. La revelación de las capas se estableció a través de un ataque químico. Una probeta no atacada revela pocos o ningún detalle estructural, a pesar de lo cual es de gran interés porque permite observar detalles que ya son visibles tales como los defectos superficiales y las inclusiones no metálicas.
El objeto de mayoría de las investigaciones metalográficas es determinar las características estructurales verdaderas de la probeta, es necesario que los diferentes constituyentes estructurales queden delineados con precisión y claridad. Esto se logra sometiendo a la probeta a la acción química de un reactivo apropiado en unas condiciones cuidadosamente controladas. El ataque químico se realizó con nital con una concentración de 2% de HNO3 diluido con 98 % de etanol o metanol de alta pureza con tiempo de exposición de aproximado de 5 s. Una sobre exposición al reactivo puede quemar la superficie de la muestra, imposibilitando la visualización de su microestructura. Asimismo, para evitar la oxidación de los especímenes se sumergieron en alcohol, agua y posteriormente se secaron con aire comprimido (libre de partículas húmedas). Las probetas pulidas pueden atacarse inmediatamente después o se puede guardar para usarla más tarde y examinarla sin ataque.
En cualquier caso, la superficie de la probeta debe protegerse de la oxidación y otros efectos perjudiciales atmosféricos. El estudio de la cinética de crecimiento, requiere de fotomicrografías de los cortes transversales de las probetas sujetas al proceso metalográfico descrito anteriormente. Utilizando un microscopio óptico de sistema invertido Olympus GX51, utilizando diferentes magnificaciones de acuerdo al tamaño de la capa borurada formada en la superficie del substrato. En la Figura 4 se presentan los pasos del proceso metalográfico para revelar la capa borurada.

Figura 4. Representación esquemática del proceso metalográfico para determinar la microestructura y la estimación del tamaño de la capa borurada formada en la superficie del hierro puro ARMCO® [83].
3.1 Observaciones microscópicas de las capas boruradas
En la Figura 5, se presentan las micrografías del hierro puro borurado con la técnica de borurización de polvo, para diferentes temperaturas y tiempos de tratamiento.
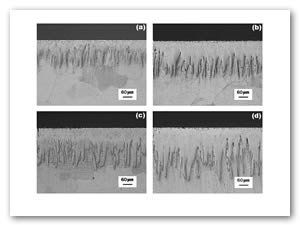
Figura 5. Morfología aserrada de la capa Fe2B formada en la superficie del hierro puro ARMCO® con la técnica de borurización en polvo con: (a) 2 h, (b) 4 h, (c) 6 h y (d) 8 h de tiempo de tratamiento a la temperatura de 1273 K.
3.2 Difracción de rayos-X
Para verificar la presencia de las fase Fe2B sobre la superficie de los aceros, se realizó un análisis por difracción de rayos X, aplicando sobre la superficie de la pieza borurada radiación CoKα con una longitud de onda de 1.7889 Å. En la Figura 6, se comprueba la presencia de la fase Fe2B.
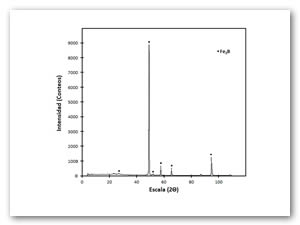
Figura 6. Patrón de difracción de rayos X originado durante la detección de la fase Fe2B en la superficie del hierro puro borurado ARMCO® con la temperatura de tratamiento de 1273 K y 8 h de tiempo de tratamiento.
La estructura cristalina para la fase Fe2B es una tetragonal centrada en el cuerpo como se presenta en la Figura 7.
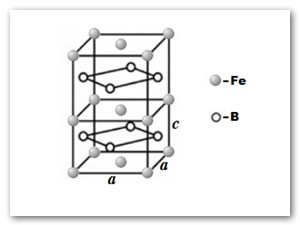
Figura 7. Estructura cristalina tetragonal centrada en el cuerpo, donde a=B=y=90° y a=b(=c), con a=0.5109nm y c=0.4249nm.
Para la estructura cristalina tetragonal centrada en el cuerpo la distancia entre los planos de la red se expresa como:
(15)
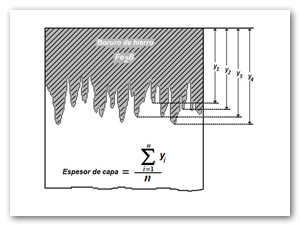
Las capas boruradas (ver Figura 5) presentan una morfología muy aserrada en la interfase de crecimiento con lo que la medición del espesor de capa no es simple [74]. La Ecuación (14), es susceptible a las mediciones de los espesores de capa. Por tal razón, se deben realizar mediciones estadísticamente confiables para determinar el coeficiente de difusión en la fase Fe2B. Para disminuir el efecto de la rugosidad en la interfase, se consideró el promedio las longitudes de cada diente como se presenta en la Figura 8 [74, 78, 79]. Las microfotografías se digitalizaron para la medición de la capa utilizando un analizador de imágenes Image Proplus, obteniendo un promedio de 100 longitudes de columnas a lo largo de la fase presente.
Resultados y discusiones
Después del proceso de borurización en polvo (empaquetamiento en caja), en la superficie de hierro puro ARMCO® se formó una sólo fase borurada (Fe2B), la cual presentan una morfología aserrada (ver Figura 5). A continuación se presenta un análisis del trabajo desarrollado por C. Martini et al. [21], donde explican el mecanismo de crecimiento de las capas boruradas aplicando el tratamiento de borurización de polvo (empaquetamiento en caja) a un hierro puro ARMCO® con un 99.9% de pureza usando diferentes mezclas de polvo con un control del potencial químico de boro. Las muestras de hierro puro fueron boruradas a la temperatura de 1123 K y un tiempo de tratamiento de 15 h usando diferentes potenciales de polvo B4C, los potenciales utilizados fueron: bajo, intermedio y alto respectivamente. Las mezclas utilizadas de carburo de boro se presentan en la Tabla 2.
Tabla 2. Potenciales químicos de carburo de boro (B4C).
| Potencial químico de boro | B4C | SiC | KBF4 |
| Bajo | 10 | 90 | - |
| Intermedio | 100 | - | - |
| Alto | 90 | - | 10 |
La considerable dilución de B4C con carburo de silicio (SiC) disminuye la tasa del potencial químico de carburo de boro y permite que las primeras etapas de crecimiento de la fase Fe2B se puedan estudiar en detalle. Con el potencial intermedio se pueden obtener capas gruesas de Fe2B. Por otra parte, para el potencial alto, el carburo de boro se mezcla con activador (KBF4) para estudiar las etapas posteriores de crecimiento, que se relacionan con la formación de bicapas (FeB-Fe2B). Durante el proceso mantienen una atmósfera controlada, sin la presencia de oxígeno ya que este reacciona con el medio borurante. Como ya se ha demostrado, el oxígeno reduce considerablemente la reactividad del hierro-boro [84].
4.1 Etapas de crecimiento de los boruros de hierro (etapa 1 de crecimiento)
Etapa 1: Cuando el substrato se mantiene en contacto con un potencial de boro bajo (ver Tabla 2), la reacción de las partículas de carburo de boro y el substrato reaccionan a un ritmo muy bajo, lo que permite observarlos con cuidado [21]. En la Figura 9(a) y (b) se presenta la morfología de los boruros de hierro sobre el substrato tratado a la temperatura de 1123 K y un tiempo corto de tratamiento de 1h. En las primeras etapas de crecimiento, cristales acirculares Fe2B crecen en direcciones radiales a partir de las zonas de contacto entre el la superficie del metal y las partículas B4C (ver Figura 9(a)). Estas características que se presentan en la etapa 1 se pueden explicar teniendo en cuanta que (i) sólo se produjeron reacciones en estado sólido y, en consecuencia átomos de boro activado fue suministrado sólo en las zonas de contacto entre la superficie del metal y las partículas de B4C.
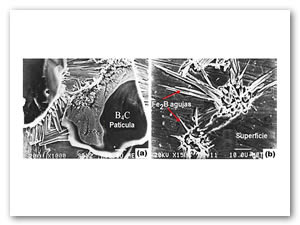
Figura 9. Muestra de hierro con tiempo de tratamiento de 1 h a la temperatura de 1123 K en contacto con potencia químico de boro bajo (ver Tabla 2): (a) imagen tomada con un microscopio electrónico de barrido de cristales de B4C (áreas obscuras) en la superficie del substrato y cristales acirculares de Fe2B creciendo sobre la superficie del metal en las zonas de contacto B4C-metal; (b) detalles del crecimiento de los cristales Fe2B en (a), después de la remoción de las partículas de carburo de boro [21]..
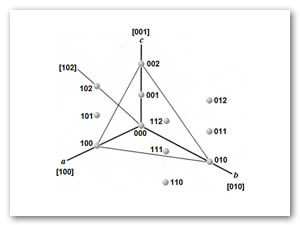
(ii) Los cristales Fe2B preferentemente crecen a lo largo de la dirección cristalográfica [001] (ver Figura 10), es decir, la dirección que tiene la distancia más corta entre los átomos vecinos de boro y, por lo tanto constituye el camino más fácil para la difusión del boro en la red tetragonal centrada en el cuerpo de la fase Fe2B; y (iii) el crecimiento de las agujas Fe2B sobre la superficie del material encuentran cada vez menos resistencia mecánica del material base, debido a un aumento considerable en el volumen (-16%) asociado con la transformación de Fe en Fe2B.
Utilizando los datos cristalográficos de la estructura cristalina tetragonal centrada en el cuerpo para la fase Fe2B ( y ), la distancia más corta entre un átomo de Fe y un átomo de B difundido en la fase Fe2B a lo largo de su trayectoria perpendicular a (001) es aproximadamente igual a 0.1902 nm (en este momento el átomo de boro B está rodeado por cuatro átomos de Fe a esta distancia; ver Figura 11(a), (b) y (c)) [31].
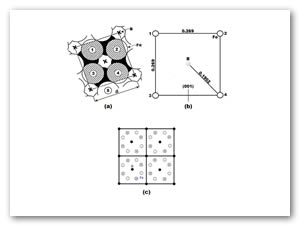
Figura 11. Proyección de los átomos de hierro Fe sobre el plano perpendicular (001) en el cual un salto atómico de B lleva a cabo en la fase Fe2B. Los puntos centrales de los átomos eclosionados están en un plano a una distancia de 3c/4 por encima del plano de proyección; los puntos centrales de los átomos obscuros están en un plano a una distancia de c/4 por encima del plano de proyección. Los radios atómicos de Fe han sido tomados igual a la mitad de la distancia más corta en la estructura Fe-Fe: 0.120 nm (por ejemplo el par de átomos 4-5 en (a)). Los átomos de B no han sido dibujados, pero las proyecciones de los átomos B coinciden con las cruces que se indican en (a). En (b) se representa la configuración del átomo de Fe alrededor del átomo de B para la fase Fe2B en el momento de máximo acercamiento durante un salto atómico de B perpendicular a (001); y finalmente en (c) representa la misma estructura de la fase Fe2B proyectada sobre el plano (001) con la colocación de los átomos en la estructura cristalina tetragonal. []= átomo de Fe en 1/4c; O= átomo de Fe en 3/4c;°= 3 átomos de B en 0, 1/2, 1c [31].
Cuando un átomo de B salta a la fase Fe2B a lo largo de la dirección cristalográfica [001] cubre una distancia de c/2 = 0.212 nm. Este tipo de crecimiento conduce a la formación de una primera capa de cristales orientados de manera diferente. Durante la primera etapa de crecimiento, algunas agujas de Fe2B también pueden crecer en el interior del substrato a lo largo de diferentes direcciones, como se muestra en la Figura 12. Estos cristales inducen en el substrato esfuerzos y distorsiones de la red cristalina los cuales son particularmente altos en las regiones del material localizadas enfrente de las puntas de las agujas [80-82]. El crecimiento de los boruros está limitado por la baja cantidad de boro activo difundido a través de la capa hasta la punta de la aguja. En esta etapa, la parte principal de boro es consumida por los cristales que crecen más rápidamente en la superficie del material.

Figura 12. Metalografía de una sección transversal de una muestra de hierro puro donde se pueden apreciar cavidades en la superficie debido al crecimiento de cristales Fe2B dentro del substrato [21].
En el trabajo de C. Martini et al. [21] reportaron que los patrones de difracción de rayos X obtenidos para una muestra de hierro a la temperatura de 1123 K con 15 h de tratamiento lo siguiente: (i) la única fase presente es la Fe2B, (ii) el mapeo del análisis de rayos X en la superficie muestra la presencia en la capa de zonas ricas en boro con las orientaciones cristalográficas (110) ó (200). Para ejemplificar el crecimiento de los boruros de hierro tipo Fe2B, en la Figura 13 se presenta la representación esquemática de la diferentes etapas de crecimiento de los cristales Fe2B: en la etapa 1, los cristales tipo Fe2B pueden crecer en diferentes zonas de la misma capa con sus ejes paralelos [001] a la superficie externa, asumiendo orientaciones las cuales pueden cambiar como consecuencia de diferencias locales en el proceso de acomodación en el metal subyacente.
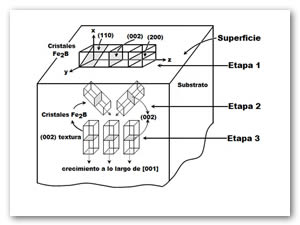
Figura 13. Representación esquemática de las etapas del crecimiento termoquímico de los cristales Fe2B: etapa 1, crecimiento sobre la superficie del material; etapa 2, crecimiento en el interior del material; etapa 3, el crecimiento profundo conduce a una fuerte orientación preferencial (002) [21].
4.2 Crecimiento de los cristales Fe2B dentro del substrato (etapa 2 de crecimiento)
El crecimiento de los cristales Fe2B dentro del substrato es predominante en esta etapa, como la demuestran los análisis de difracción de rayos X llevado a cabo por C. Martini et al. [21], en capas de 15 a 50 μ, la única fase presente a la misma temperatura utilizando un potencial químico intermedio es la fase Fe2B. Los patrones reportados muestran que existe una orientación preferencial (002) cuya fuerza aumenta a medida que la profundidad del análisis se incrementa. En particular, el crecimiento de los boruros cerca de la interfase Fe2B/substrato sólo muestra el pico de difracción (002) de Fe2B. La segunda etapa de crecimiento Fe2B se caracteriza por la transición de una capa delgada externa con regiones de cristales orientados al azar o de carácter local (110) ó (200), a una región interna gruesa y compacta con orientaciones cristalográficas (002).
Debido a que la superficie del substrato está cubierta por las partículas de B4C, hay un incremento en el número de cristales (creciendo sobre la superficie del material a lo largo de la dirección [001]), que entran en contacto con, cristales no paralelos adyacentes, además se someten a fuertes esfuerzos mecánicos. Debido a estos obstáculos, algunos cristales detienen su crecimiento (Figura 14(a)), mientras que otros cristales sólo pueden crecer después de cambiar de dirección en la superficie del substrato (ver Figura 14(b)). En esta etapa, esquematizado en la Figura 14, (etapa 2), un número cada vez mayor de cristales se ven obligados a crecer dentro del material, es decir, a la dirección [001], eje de fácil crecimiento no paralelo a la superficie del marial. Por otra parte, el crecimiento de las agujas de los boruros dentro del substrato se ven favorecidos por el hecho de que la cantidad de boro consumido por el crecimiento de los cristales en la superficie del substrato disminuye y, en consecuencia, más boro puede difundirse hacia las puntas de las agujas de crecimiento.

Figura 14. Micrografías con la técnica de Microscopia Electrónica de Barrido (SEM) de cristales Fe2B creciendo en la superficie del metal, donde (a) detenido, o (b) forzado a cambiar de dirección como consecuencia de estar en contacto con cristales adyacentes [21].
4.3 Establecimiento de una fuerte textura Fe2B en (002) (etapa 3 de crecimiento)
Durante la etapa 2 de crecimiento varios cristales Fe2B creciendo a lo largo de diferentes direcciones pueden entrar en contacto entre sí. En consecuencia, un número cada vez mayor de cristales se ve obligado a crecer a lo largo de una dirección de resistencia mínima, es decir, en la dirección [001]. Por lo tanto, una tercera etapa de crecimiento, se produce en todas las agujas de los boruros que tienden a crecer de forma perpendicular a la superficie externa (Figura 13, etapa 3). Esto explica plenamente (i) la formación de cristales Fe2B orientados con sus planos (002) paralelos a la superficie externa, y (ii) el incremento de esta orientación con respecto a la profundidad de la capa (interfase de crecimiento) aumenta.
4.4 Adherencia de la capa borurada
Una de las propiedades básicas de un compuesto capa-sustrato funcional es una suficiente adherencia de la capa sobre el substrato. La necesidad de la medición de la calidad y la resistencia adhesiva del sistema en la práctica ya se ha llevado a cabo a través de métodos de ensayo simples como la indentación Daimler-Benz Rockwell C en una superficie recubierta. Este método de ensayo es fácil de manejar, pero sólo da ideas cualitativas de adhesión. Se utilizó un indentador cónico de diamante con una punta de 200 µm de radio, 1.5 cm de altura. Se realizaron tres conjuntos de indentaciones sobre la cara recubierta, con una carga de 150 kg. En la Figura 15 se presenta una huella observada con Microscopía Electrónica de Barrido (SEM) para evaluar el daño del recubrimiento debido por la carga aplicada.

Figura 15. Micrografía con la técnica de Microscopia Electrónica de Barrido (SEM) mostrando la indentación de una prueba de adhesión VDI del hierro puro borurado a la temperatura de tratamiento de 1273 K y 4 h.
Los diferentes tipos de daño observados son comparados con los estados convencionales de calidad de adherencia, que se posicionan sobre una escala HF (de HF1 a HF6) (ver Figura 16) que representa la fuerza de adherencia entre el sustrato y el recubrimiento. Entre HF1 y HF4 la adherencia es suficiente, mientras que HF5 y HF6 representan una adherencia insuficiente. Analizando la Figura 15, se puede determinar que representa una HF3, mostrando una adherencia suficiente de la capa borurada sobre el substrato.
Continuando con el análisis de los resultados, en las Tabla 3, se presentan los resultados de los espesores obtenidos de la medición de las capas boruradas en la fase Fe2B para el proceso de borurización en polvo del hierro puro ARMCO®.
Tabla 3.Resultados experimentales de los espesores (µm) de capa de la fase Fe2B con la técnica de borurización de empaquetamiento en caja.
| Tiempo (h) | Temperatura 1123(k) | Temperatura 1173(k) | Temperatura 1223(k) | Temperatura 1273(k) |
| 2 | 40.34 ± 7.70 | 59.50 ± 12.2 | 84.11 ± 15.5 | 109.5 ± 23.6 |
| 4 | 61.48 ± 10.1 | 96.10 ± 13.9 | 128.2 ± 17.5 | 116.8 ± 27.3 |
| 6 | 77.02 ± 13.8 | 115.1 ± 14.4 | 160.6 ± 19.2 | 209.0 ± 25.3 |
| 8 | 89.92 ± 16.4 | 137.4 ± 17.5 | 187.5 ± 25.7 | 244.0 ± 29.5 |
Con la consideración de estos resultados (ver Tabla 3), se procedió a la evaluación del modelo presentado. De acuerdo con la Ecuación
(10)
se graficó vs. como se puede apreciar en la Figura 17.
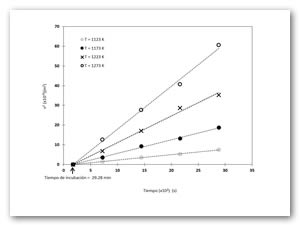
Figura 17. El cuadrado de los espesores de las capas boruradas (v2) como función del tiempo de tratamiento (t) (ver Ecuación (10)) con la técnica de borurización de empaquetamiento en caja.
Las pendientes de las líneas rectas de la Figura 17, representan las constantes de crecimiento parabólico de la Ecuación (10)
![]()
La nucleación del boruro de hierro en la interfase gas/sólido sólo toma lugar después de que la concentración de boro en esta interfase excede un valor crítico Cads>CupFe2B[55]. La acumulación de boro en la interfase gas/sólido tiene que ver con la adsorción natural de los átomos de boro, en el interior del material, todos los enlaces químicos (metálicos) de los átomos de hierro están satisfechos. En cambio por definición la superficie representa una discontinuidad de esos enlaces. Para esos enlaces incompletos, es enérgicamente favorable el reaccionar con lo que se encuentra disponible, y por ello se produce de forma espontánea. En el periodo de incubación del boruro de hierro (t0Fe2B=29.28min), se forma una película base (v0), la cual termina con la aparición de los primeros boruros de hierro y justamente es en la intercepción con el eje de las abscisas en el gráfico de v2 vs. t. En la Tabla 4 se presentan las constantes de crecimiento parabólico respecto a cada temperatura obtenidas de la Figura 17. Asimismo, se menciona el valor del parámetro de normalización de crecimiento de la fase Fe2B obtenido de la Ecuación (14).
Tabla 4 Parámetro de normalización de crecimiento y constantes de crecimiento como una función de la temperatura de tratamiento.
| Temperatura (k) | E2 (Adimensional) | 4E2DFe2B (m2s-1) | Coeficiente de difusión (m2s-1) |
| 1123 | --- | 2.99x10-13 | 4.61x10-11 |
| 1173 | 1.61975x10-12 | 7.00x10-13 | 1.08x10-10 |
| 1223 | --- | 1.29x10-12 | 2.00x10-10 |
| 1273 | --- | 2.20x10-12 | 3.99x10-10 |
Asumiendo un comportamiento Arrheius de los coeficientes de difusión presentados en la Tabla 4, la energía de activación QFe2B es obtenida de la pendiente del gráfico que se presenta en la Figura 18. A partir de la ecuación del ajuste de la Figura 18, se expresa el coeficiente de difusión (Fe2b ) vía la relación de Arrhenius (DFe2B=D0exp(-Q/TR)) para los procesos de borurización en el rango de temperaturas de tratamiento de 1123 ≤ T ≤ 1273 K en el hierro puro ARMCO® como:
(16)
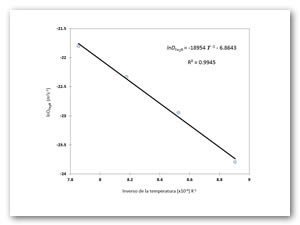
Figura 18. La pendiente de InDFe2B vs.1/T determinan la energía de activación QFe2B en el hierro puro ARMCO®.
De la Ecuación (16), R es la constante universal de los gases (= 8.314 J/mol K), y T representa la temperatura absoluta (K). El valore de la energía de activación[10] QFe2B indican la energía necesaria para estimular la difusión de boro a lo largo de la dirección cristalográfica [001] en la fase Fe2B. Considerando la expresión para el coeficiente de difusión del boro en la Ecuación (16), es posible expresar la ley de crecimiento parabólico (ver Ecuación (10)) como sigue:
(17)
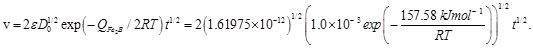
Para validar el modelo de difusión, se boruro el hierro puro ARMCO® a la temperatura de 1253 K para 5 h de tiempo de tratamiento (ver Figura 19).
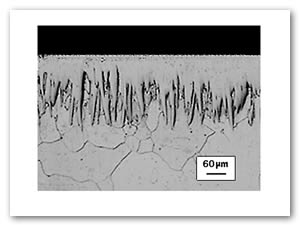
Figura 19. Morfología aserrada de la capa Fe2B formada en la superficie del hierro puro ARMCO® a 1253 K de temperatura con 5 h de tiempo de tratamiento [87].
Los resultados obtenidos de la Ecuación (17), son comparados con los valores experimentales para validar el modelo de difusión como se muestra en la Tabla 5.
Tabla 5. Comparación de los espesores de capa experimental y el estimado a partir de la Ecuación (17), con una temperatura de tratamiento de 1253 K y 5 h de tratamiento.
| Temperatura (k) | Espesor de capa experimental (µm) | Espesor de capa estimado de la Ec.(17) (µm) |
| 1253 | 175.25 ± 12.5 | 181.16 |
El modelo de difusión presentado en la Ecuación (17) tiene una amplia aplicabilidad y puede ser utilizado para estimar el espesor de capa borurada óptimo para diferentes aleaciones ferrosas y no ferrosas. Sin embargo, existe muy poca literatura relacionada con la modelación del crecimiento de las capas boruradas que consideren los diferentes parámetros que intervienen en el proceso. En la práctica existen diferentes aplicaciones relacionadas con la profundidad de la capa borurada [1]. Los espesores de capa aconsejables según la aplicación, capas delgadas (por ejemplo, de 15 a 20 μm) son usadas para proteger el substrato en contra del desgaste adhesivo (tales como desprendimiento y formación de viruta, troqueles estampadores de metal y herramientas), mientras que capas gruesas son recomendables para disminuir el desgaste abrasivo (herramentales de extrusión para plástico con cargas abrasivas y herramentales de prensa para la industria cerámica). En el caso de aceros de bajo carbono[11] y aceros de baja aleación [12], el rango óptimo de espesor de capa borurada es de 50 a 250 μm, y para aceros de alto carbono [13] y aceros de alta aleación[14], el rango óptimo de espesor de capa borurada es de 25 a 76 μm. Asimismo, este modelo puede ser extendido para predecir la cinética de crecimiento de bicapas (FeB-Fe2B) en la superficie de diferentes aleaciones ferrosas.
Conclusiones
La cinética de crecimiento de las capas Fe2B formadas en la superficie del hierro puro ARMCO® fue estimada para el proceso de borurización en polvo usando un modelo de difusión. El modelo considera la influencia del tiempo de incubación, tiempo y temperatura de tratamiento. Se asumió que las capas obedecen la ley de crecimiento parabólico. Finalmente, el modelo de difusión desarrollado, fue comprobado para este proceso, esto permite que pueda ser utilizado para estimar los espesores de las capas boruradas en diferentes aleaciones ferrosas y no ferrosas para un conjunto de condiciones experimentales, lo que permitirá facilitar la optimización y automatización de los procesos de borurización.
Agradecimientos
El trabajo descrito en el presente artículo fue financiado por la beca otorgada por PROMEP. Asimismo, le agradezco al Ing. Martín Ortiz Granillo, quien es Director de la Escuela Superior de Ciudad Sahagún-UAEH, México, por todas las facilidades para concluir este trabajo de investigación.
Referencias
1. A. Graf von Matuschka, Boronizing, Second ed., Carl Hanser Verlag, Munich, 1980.
2. Walter Fichtl, Boronizing and its Practical Applications. Materials in Engineering, 2 (1981), 276–286.
3. S. C. Singhal, A hard diffusion boride coating for ferrous materials, Thin Solid Films, 45 (1977), 321–329.
4. E. Takeuchi, Sliding wear characteristics of gas boronized steel, Wear, 55 (1979), 121–130.
5. D. Teneva, Increasing the wear resistance of rings for spinning machines through boriding, Journal of the Less Common Metals, 67 (1979), 493–497.
6. K. H. Habig, Wear Protection of Steels by Boriding,Vanadizing, Nitriding, Carburising, and Hardening, Materials in Engineering, 2 (1980), 83–91.
7. K. H. Habig and R. Chatterjee-Fischert, Wear behaviour of boride layers on alloyed steels, Tribology international, 14 (1981), 209–215.
8. N. Bozkurt, A. E. Gekinli, M. Gekinli, Autoradiographic Study on Boronized Steel, Materials Science and Engineering, 57 (1983), 181–186.
9. D. N. Tsipas, H. Noguera and Rus, Corrosion behaviour of boronized low carbon steel, Materials Chemistry and Physics, 18 (1987), 295–668.
10. A. G. Wang and I. M. Hutchings, Mechanisms of abrasive wear in a boronized alloy steel, Wear, 124 (1988), 149–163.
11. Sharon Alwart, Claus-Peter Ulrich, Abrasive resistant hard steel surfaces produced by boriding, Industrial Heating, 65 (1998), 47–50.
12. B. Selcuk, R. Ipek, M. B. Karamis, V. Kuzucu, An investigation on surface properties of treated low carbon and alloyed steels (boriding and carburizing), Journal of Materials Processing Technology, 103 (2000), 310–317.
13. Cevdet Meric, Salim Sahina, Selim Sarper Yilmazb, Investigation of the effect on boride layer of powder particle size used in boronizing with solid boron-yielding substances, Materials Research Bulletin, 35 (2000), 2165–2172.
14. R. Ipek, B. Selcuk, M. B. Karamis, V. Kuzucu, A. Yucel, An evaluation of the possibilities of using borided GG25 cast iron instead of chilled GG25 cast iron (surface properties), Journal of Materials Processing Technology, 105 (2000), 73–79.
15. Enver Atık, Umut Yunker, Cevdet Merıc, The effects of conventional heat treatment and boronizing on abrasive wear and corrosion of SAE 1010, SAE 1040, D2 and 304 steels, Tribology International, 36 (2003), 155–161.
16. M. González Fernández de Castro, Boración de aceros. Tesis de Doctorado, Universidad Politécnica de Madrid, España, 1999.
17. C. I. Villa Velázquez, Estudio del agrietamiento tipo Palmqvist y evaluación de esfuerzos residuales en aceros AISI 1018. Tesis de Doctorado, SEPI-ESIME Zacatenco, Instituto Politécnico Nacional, México, 2009.
18. T. B. Massalski, Binary Alloys Phase diagrams, second ed., ASM International, USA, 1990.
19. T. Van Rompaey, K. C. Hari Kumar, P. Wollants, Thermodynamic Optimization of the B-Fe System, J. Alloys Comp, 334 (2002) 173–181.
20. H. Okamoto, B-Fe (Boron-Iron), J. Phase Eq. Diff. 25 (2004) 297–298.
21. C. Martini, G. Palombarini, and M. Carbucicchio, Mechanism of thermochemical growth of iron borides on iron, J. Mater. Sci. 39 (2004), 933–937.
22. P. Goeuriot, F. Thevenot and J. H. Driver, Surface treatment of steels: Borudif, a new boriding process, Thin Solid Films, 78 (1981), 67–76.
23. P. Goeuriot, R. Fillit, F. Thevenot, J. H. Driver and H. Bruyas, The Influence of Alloying Element Additions on the Boriding of Steels, Materials Science and Engineering, 55 (1982), 9–19.
24. M. Carbucicchio and G. Palombarini, Effects of alloying elements on the growth of iron boride coatings , Journal of Materials Science Letters, 6 (1987), 1147–1149.
25. Sukru Taktak, A study on the diffusion kinetics of borides on boronized Cr-based steels, J. Mater Sci., 41 (2006), 7590–7596.
26. I. Campos-Silva, M. Ortiz-Domínguez, O. Bravo-Bárcenas, M. A. Doñu-Ruiz, D. Bravo-Bárcenas, C. Tapia-Quintero and M. Y. Jiménez-Reyes, Formation and kinetics of FeB/Fe2B layers and diffusion zone at the surface of AISI 316 borided steels, Surface and Coatings Technology, 205 (2010), 403–412.
27. J. R. Davis: Surface Hardening of Steels: Understanding the Basics, 1st. edn., 2002, USA, ASM International.
28. J. R. Davis: Surface Hardening of Steels: Understanding the Basics, 1st. edn., 2002, USA, ASM International.
29. I. Campos-Silva, M. Ortiz-Domínguez, H. Cimenoglu, R. Escobar-Galindo, M. Keddam, M. Elias-Espinosa, N. López-Perrusquia, A diffusion model for the growth of the Fe2B layer in pure iron, Surface Engineering, 27 (2011) 189-195.
30. M. Ortiz-Domínguez, E. Hernández-Sánchez, J. Martínez-Trinidad, M. Keddam, I. Campos-Silva, A kinetic model for analyzing the growth kinetics of Fe2B layers in AISI 4140 steel, Kovove Mater., 48 (2010), 1–6.
31. C. M. Brakman, A. W. J. Gommers, and E. J. Mittemeijer, Bonding of Fe and Fe-C, Fe-Cr, and Fe-Ni alloys; Boride-layer growth kinetics, J. Mater. Res., 4 (1989), 1354–1370.
32. T. C. Lei, B. L. Jiang and W. Liu, Effect of cold deformation on boronizing processes and wear behavior of low carbon steel AISI 1020, Materials Chemistry and Physics, 26 (1990), 445–454.
33. Joshua Pelleg and M. Judelewicz, Diffusion in the B-Fe system and compound formation between electron gun deposited boron thin films and steel substrate, Thin Solid Films, 215 (1992), 35–41.
34. A. Ozsoy, Y. M. Yaman, The effect of thermocycling liquid boronizing on the thickness of the boride layer and the transition zone, Scripta Metallurgica, et Materialia, 29 (1993), 231–236.
35. Wendong Wang, Sanhong Zhang and Xinlai He, Diffusion of boron in alloys, Acta Metall, Mater. 43 (1995), 1693–699.
36. C. H. Xu, J. K. Xi and W. Gao, Isothermal superplastic boronizing of high carbon and low alloy steels, Scripta Materialia, 34 (1996), 455–461.
37. Karlo Raic, Zorica Acimovic, Nada Vidojevic and Nada Novovic-Simovic, Modelling of Fe2B boride layer growth, J. Serb. Chem. Soc., 61 (1996), 181–188.
38. E. Meléndez, I. Campos, E. Rocha, M. A. Barron, Structural and strength characterization of steels subjected to boriding thermochemical process, Materials Science and Engineering, A 234-236 (1997), 900–903.
39. Fan-Shiong Chen, Kuo-Liang Wang, The kinetics and mechanism of multi-component diffusion on AISI 1045 steel, Surface and Coatings Technology, 115 (1999), 239–248.
40. J. H. Yoon, Y. K. Jee, S. Y. Lee, Plasma paste boronizing treatment of the stainless steel AISI 304, Surface and Coatings Technology, 112 (1999), 71–75.
41. Kenan Genel, Ibrahim Ozbek, Akif Kurt, Cuma Bindal, Boriding response of AISI W1 steel and use of artificial neural network for prediction of borided layer properties, Surface and Coatings Technology, 160 (2002), 38–43.
42. I. Campos, J. Oseguera, U. Figueroa, J. A. García, O. Bautista, G. Kelemenis, Kinetic study of boron diffusion in the paste-boriding process, Materials Science and Engineering A, 352 (2003), 261–265.
43. K. Genel, I. Ozbek, C. Bindal, Kinetics of boriding of AISI W1 steel, Materials Science and Engineering, A 347 (2003), 311–314.
44. U. Yapar, C. F. Arısoy, G. Basman, S. A. Yesilcubuk and M. K. Sesen, Surface Modification of En-C35E Steels by Thermo-Chemical Boronizing Process and its Properties, Key Engineering Materials, 264-268 (2004), 633–636.
45. ] V. V. Shyrokov, K. B. Vasyliv, and L. A. Arendar, Specific features of the borating of iron–carbon alloys in sodium melt, Materials Science, 40 (2004), 270–276.
46. S. Sen, U. Sen and C. Bindal, Kinetics of Boride Layers Formed on the Surface of AISI 4140 Steel, Key Engineering Materials, 264-268 (2004), 565–568.
47. M. Keddam, A kinetic model for the borided layers by the paste-boriding process, Applied Surface Science, 236 (2004), 451–455.
48. V. I. Dybkov, W. Lengauer, K. Barmak, Formation of boride layers at the Fe–10% Cr alloy–boron interfase, Journal of Alloys and Compounds, 398 (2005), 113–122.
49. L. G. Yu , X. J. Chen, K. A. Khor, G. Sundararajan, FeB/Fe2B phase transformation during SPS pack-boriding: Boride layer growth kinetics, Acta Materialia, 53 (2005), 2361–2368.
50. Saduman Sena, Ugur Sen, Cuma Bindal, An approach to kinetic study of borided steels, Surface and Coatings Technology, 191 (2005), 274–285.
51. Rafidah Hasan, Iswadi Jauhari, Syahrizad Mohd Yunus, Rd. Dadan Ramdan and Nik Rozlin Nik Masdek, Surface properties and kinetics of boronized duplex stainless steel, Proceedings of the International Conference on Recent Advances in Mechanical and Materials Engineering, 128 (2005), 30–31.
52. Saduman Sena, Ugur Sena, Cuma Bindal, The growth kinetics of borides formed on boronized AISI 4140, Vacuum, 77 (2005), 195–202.
53. I. Campos, O. Bautista, G. Ramírez, M. Islas, J. De La Parra, L. Zuñiga, Effect of boron paste thickness on the growth kinetics of Fe2B boride layers during the boriding process, Applied Surface Science, Volume 243 (2005), 429–436.
54. M. Keddam, S. M. Chentouf, A diffusion model for describing the bilayer growth (FeB/Fe2B) during the iron powder-pack boriding, Applied Surface Science, 252 (2005), 393–399.
55. L. G. Yu, K. A. Khor, G. Sundararajan, Boride layer growth kinetics during boriding of molybdenum by the Spark Plasma Sintering (SPS), Surface and Coatings Technology, 201 (2006), 2849–2853.
56. V. I. Dybkov, W. Lengauer P. Gas, Formation of boride layers at the Fe–25% Cr alloy–boron Interfase, J Mater Sci., 41 (2006), 4948–4960.
57. I. C. Elikyureka, B. Baksana, O. Torunb, R. Gurlera, Boronizing of iron aluminide Fe72Al28, Intermetallics, 14 (2006), 136–141.
58. M. Keddam, Computer simulation of monolayer growth kinetics of Fe2B phase during the paste-boriding process: Influence of the paste thickness, Applied Surface Science, 253 (2006), 757–761.
59. I. Campos, R. Torres, G. Ramírez, R. Ganem, J. Martínez, Growth kinetics of iron boride layers: Dimensional analysis, Applied Surface Science, 252 (2006), 8662–8667.
60. I. Campos, R. Torres, O. Bautista, G. Ramírez, L. Zúñiga, Effect of boron paste thickness on the growth kinetics of polyphase boride coatings during the boriding process, Applied Surface Science, 252 (2006), 2396–2403.
61. K. Genel, Boriding kinetics of H13 steel, Vacuum, 80 (2006), 451–457.
62. I. Uslu, H. Comert, M. Ipek, F. G. Celebi, O. Ozdemir, C. Bindal, A comparison of borides formed on AISI 1040 and AISI P20 steels, Materials and Design, 28 (2007), 1819–1826.
63. Lingyun Xu, Xiaochun Wuy and Hongbin Wang, Influence of Surface Nano-structured Treatment on Pack Boriding of H13 Steel, J. Mater. Sci. Technol., 23 (2007), 525–528.
64. S. Taktak, Characterization of pack borided AISI 4140 steel after nickel electroplating, Kovove Mater., 45 (2007), 215–222.
65. I. Campos, M. Islas, G. Ramírez, C. VillaVelázquez, C. Mota, Growth kinetics of borided layers: Artificial neural network and least square approaches, Applied Surface Science, 253 (2007), 6226–6231.
66. R. Torres, I. Campos, G. Ramírez, O. Bautista and J. Martínez, Dimensional analysis in the growth kinetics of FeB and Fe2B layers during the boriding process, Int. J. Microstructure and Materials Properties, 2 (2007), 73–83.
67. I. Campos, G. Ramírez, U. Figueroa, J. Martínez, O. Morales, Evaluation of boron mobility on the phases FeB, Fe2B and diffusion zone in AISI 1045 and M2 steels, Applied Surface Science, 253 (2007), 3469–3475.
68. V. I. Dybkov, Growth of boride layers on the 13% Cr steel surface in a mixture of amorphous boron and KBF4, J Mater Sci., 42 (2007), 6614–6627.
69. I. Campos, G. Ramírez, U. Figueroa and C. Villa Velázquez, Paste boriding process: evaluation of boron mobility on borided steels, Surface Engineering, 23 (2007), 216–222.
70. X. J. Chen, L. G. Yu, K. A. Khor, G. Sundararajan, The effect of boron-pack refreshment on the boriding of mild steel by the spark plasma sintering (SPS) process, Surface and Coatings Technology, 202 (2008), 2830–2836.
71. M. Keddam, Growth Kinetics of Fe Boride Layers: Application of a Diffusion Model, Defect and Diffusion Forum, 273–276 (2008), 318–322.
72. I. Campos-Silva, A. S. Balankin, A. H. Sierra, N. López-Perrusquia, R. Escobar-Galindo, D. Morales-Matamoros, Characterization of rough interfases obtained by boriding, Applied Surface Science, 255 (2008), 2596–2602.
73. Gözde Çelebi Efe, Mediha İpek, İbrahim Özbek, Cuma Bindal, Kinetics of borided 31CrMoV9 and 34CrAlNi7 steels, Materials Characterization, 59 (2008), 23–31.
74. O. Culha, M. Toparlia, S. Sahinb, T. Aksoya, Characterization and determination of FexB layers mechanical properties, Journal of Materials Processing Technology 206 (2008), 231–240.
75. Naruemon Suwattananont, E. Roumiana, S. Petrova, Oxidation Kinetics of Boronized Low Carbon Steel AISI 1018, Oxid. Met., 70 (2008), 307–315
76. O. Torun, Boriding of nickel aluminide, Surface and Coatings Technology, 202 (2008), 3549–3554.
77. O. Ozdemir, M. A. Omar, M. Usta, S. Zeytin, C. Bindal, A. H. Ucisik, An investigation on boriding kinetics of AISI 316 stainless steel, Vacuum, 83 (2009), 175–179.
78. I. Campos-Silva, M. Ortiz-Domínguez, M. Keddam, N. López-Perrusquia, A. Carmona-Vargas, M. Elias-Espinosa, Kinetics of the formation of Fe2B layers in gray cast iron: Effects of boron concentration and boride incubation time, Applied Surface Science, 255 (2009) 9290–9295.
79. I. Campos-Silva, M. Ortiz-Domínguez, N. López-Perrusquia, A. Meneses-Amador, R. Escobar-Galindo, J. Martínez-Trinidad, Characterization of AISI 4140 borided steels, Applied Surface Science, 256 (2010) 2372–2379.
80. L. Elsgoltz, Ecuaciones diferenciales y cálculo variational, 3ra edición. Editorial Mir, Moscú, 1983.
81. N. López Perrusquia, Evaluación de la tenacidad a la fractura por microindentación en aceros borurizados AISI 4140. Tesis de Maestría, SEPI-ESIME Azcapotzalco, Instituto Politécnico Nacional, México, 2008.
82. C. I. Villa Velázquez, Estudio del agrietamiento tipo Palmqvist y evaluación de esfuerzos residuales en aceros AISI 1018. Tesis de Doctorado, SEPI-ESIME Zacatenco, Instituto Politécnico Nacional, México, 2009.
83. D. I. B. Barcenas, Caracterización mecánica y estructural de una aleación Co-Cr-Mo ASTM F-75 endurecida superficialmente por difusión de boro. Tesis de Doctorado, SEPI-ESIME Zacatenco, Instituto Politécnico Nacional, México, 2014.
84. G. Palombarini, G. Sambogna and M. Carbucicchio, Role of oxygen in iron boriding using boron carbide, Journal of Materials Science Letters, 12 (1993), 741–742.
85. Verein Deutscher Ingeniure Normen, VDI 3198. VDI-Verlag, Dusseldorf, (1991), 1-8.
86. N. Vidakis, A. Antoniadis, and N. Nilalis, The VDI, 3198 Indentation Test Evaluation of a Reliable Qualitative Control for Layered Compounds, J. Mater. Porocess. Technol, 143-144 (2003), 481-485.
87. M. Elias-Espinosa, M. Ortiz-Domínguez, M. Keddam, M. A. Flores-Rentería, O. Damián-Mejía, J. Zuno-Silva, J. Hernández-Ávila, E. Cardoso-Legorreta, A. Arenas-Flores, Growth kinetics of the Fe2B layers and adhesión on Armco iron substrate, Journal of Materials Engineering and Performance, 23 (2014), 2943-2952.
[1]El radio atómico de un átomo de boro es de 87x10-12 m.
[2]El radio atómico de un átomo de hierro es de 155.8x10-12m.
[3]La textura es la disposición y el orden de los cristales en la fase Fe2B.
[4]La coalescencia es la capacidad de dos o más materiales de unirse en un único cuerpo.
[5]Gestación es el tiempo que dura el boruro de hierro en el desarrollo y varía entre las diferentes fases (FeB y Fe2B).
[6]Ésta es la forma estable del hierro puro a temperaturas que oscilan entre los 900 a 1400 oC. La austenita es blanda y dúctil y, en general, la mayoría de las operaciones de forja y laminado de aceros se efectúa a aproximadamente los 1100 oC.
[7]En el tiempo de incubación, se forma una película base, la cual termina con la aparición de los primeros boruros de hierro.
[8]La solubilidad es una medida de la capacidad de disolverse una determinada sustancia (átomos de boro) en un determinado solvente (substrato).
[9]B4C + 4KBF4 + 3SiC +2O2 → 8B + 4KF + 3SiF4 + 4CO, B4C + 4KBF4 + 3SiC +3O2 → 6B + 4KF + 3SiF4 + 4CO + B2O2
[10]Un átomo que se difunde debe escurrirse entre los átomos circundantes para ocupar su nueva posición. El átomo que se difunde, debe atravesar una barrera de energía potencial (energía de activación).
[11]El carbono tiene una gran influencia en el comportamiento mecánico de los aceros, tienen menos del 0.25 wt. % C en su aleación.
[12]Los aceros de baja aleación tienen menos que el 5 wt. % de elementos de aleación.
[13]Los aceros de alto carbono, tienen entre 0.6 y 1.2 wt. % C en su aleación.
[14]Los aceros de alta aleación tienen mayor que el 10 wt. % de elementos de aleación.
[a] Profesor de la Universidad Autónoma del Estado de Hidalgo.