Autocuidados de la mujer embarazada en el consumo de antiemeticos (doxilamina / piridoxina y metoclopramida)
Resumen
Antecedentes: La náusea sola o en combinación con vómitos puede presentarse en el embarazo (NVE). La náusea es un trastorno común que afecta el 50-70 % de las mujeres embarazadas. NVE es característica del primer trimestre. Alrededor del 2 % de las mujeres embarazadas experimentan la forma más grave de NVE, es la hiperémesis gravídica. Esta patología reduce sustancialmente la calidad de vida de la mujer embarazada. Se puede requerir una intervención con antieméticos hasta que desaparezca.
Objetivos: Investigar el porcentaje de mujeres que toman antieméticos durante el embarazo, analizar el potencial riesgo teratogénico y establecer estrategias para el autocuidado.
Material y métodos: Se analizaron los datos del Estudio Colaborativo Español de Malformaciones Congénitas de red (ECEMC). Se consideraron como expuestos los lactantes (casos y sus controles) cuyas madres estuvieron expuestas a fármacos antieméticos, durante el primer trimestre del embarazo. Para el análisis de fármacos antieméticos, se consideraron los datos de combinación de doxilamina/piridoxina, metoclopramida y el subgrupo de fenotiazinas (OR=1.69, p=0.017).
Resultados: Los datos registrados en el ECEMC un promedio de 49 % de las mujeres embarazadas se ha reportado NVE. El antiemético más consumido fue doxilamina/piridoxina. La metoclopramida fue el segundo antiemético consumido y con pocos casos expuestos el subgrupo fenotiazinas. La combinación de doxilamina / piridoxina no presentó riesgo en la población de mujeres embarazadas españolas (OR=1.02, p = 0.36). La metoclopramida mostró un pequeño pero significativo aumento del riesgo teratogénico (OR = 1.21, p=0.0001), así como las fenotiazinas (OR=1.69, p=0.017).
Conclusiones: El impacto de NVE en la salud se relaciona con una baja calidad de vida en las mujeres embarazadas y que tiende a ser minimizado. Esta es la razón por la que debemos tratar a NVE en forma oportuna con medicamentos seguros. Los autocuidados durante el embarazo deben ser mayores y no permitir las complicaciones de la NVE. La combinación de doxilamina / piridoxina usado durante el primer trimestre de embarazo no se asoció con un mayor riesgo de malformaciones.
Palabras clave: Nauseas, vómitos, embarazo, autocuidados, antieméticos, teratogenos..
Abstract
Background: Nausea alone or in combination with vomiting during pregnancy is a common disorder affecting 50-70% of pregnant women. Nausea and vomiting in pregnancy (NVP) are common features of the first trimester. About 2 % of pregnant women experience the most severe form of NVP, it is hyperemesis gravidarum. This pathology substantially reduces the pregnant woman´s life quality. It may require intervention with anti-emetics until subsides.
Methods: We analyzed the data from the Spanish Collaborative Study of Congenital Malformations (ECEMC) network. We considered as exposed those infants (cases and its controls) whose mother were exposed to antiemetic drugs, at least during the first trimester of pregnancy. For the analysis of antiemetic drugs, we considered the data of combination doxylamine/pyridoxine, metoclopramide and phenotiazines subgroup.
Results: Data registered in ECEMC an average of 49% of pregnant women has been reported NVP. The most widely consumed antiemetic was doxylamine/pyridoxine. Metoclopramida was the second antiemetic consumed and with few exposed cases the Phenotiazines subgroup. The combination of doxylamine/pyridoxine did no cause an increased risk in the population of pregnant Spanish women (OR= 1.02, p= 0.36). Metoclopramide showed a small but significant increase in teratogenic risk (OR= 1.21, p= 0.0001), as phenothiazines (OR= 1.69, p= 0.017).
Conclusions: The impact of NVP on health is related with low quality of live in pregnant women and it tends to be minimized. This is the reason why we should treat NVP in a timely form with safe medications. The autocare in pregnancy must be majors and we don´t permit complications of NVP. The combination doxylamine/pyridoxine used during the first trimester of pregnancy may not to be associated with an increased risk for malformations.
Keywords: Nausea, vomiting, pregnancy, autocare, antiemetics, teratogen.
Introducción
Las náuseas y los vómitos (NVE) son características comunes del primer trimestre que se dan por sentadas por la mayoría de las mujeres. [1] Las náuseas del embarazo son con frecuencia un síntoma de diagnóstico precoz del embarazo normal, [2] suelen considerarse simplemente como un efecto desagradable y con frecuencia incapacitante del embarazo. [3]
Prevalencia
Las náuseas solas o en combinación con vómitos durante el embarazo es un trastorno común que afecta a entre el 50% y 80% de las mujeres embarazadas, por lo general ocurren al comienzo del embarazo y disminuyen a principios del segundo trimestre. [3]
NVE son un importante problema de salud en el embarazo [4] y afectan a 4 millones de mujeres embarazadas aproximadamente en EE.UU. y 350, 000 en Canadá, equivalente al 80% del total. [5] Esto significa que más de la mitad de las mujeres con embarazos sin complicaciones sufren de NVE. [6]
Hasta un 80% de la emesis gravídica en las mujeres embarazadas se experimenta en el primer trimestre. En alrededor del 20% de los embarazos estos síntomas continúan más allá de la semana 14 y persisten durante todo el embarazo. En aproximadamente 3 por cada 1.000 embarazos el vómito se convierte en hiperémesis gravídica severa (HG). [2]
Otros autores refieren que aproximadamente 1,5 a 2% de las mujeres embarazadas experimentan la forma más grave de NVP, la hiperémesis gravídica [7] que pueden interferir con la nutrición y la ingesta de líquidos. Esta patología es la causa más frecuente de hospitalización en el primer trimestre del embarazo, y puede ser prevenida con medicamentos anti-eméticos. [8]
Etiología
Poco se sabe acerca de la etiología, la causa y posible función de esta condición, aunque se cree que las hormonas de la madre y de la placenta participan en la etiología de la emesis gravídica. [9] Se produce, probablemente, por el aumento de los niveles de las hormonas gonadotrofinas y la tiroides, alteraciones en el ritmo gástrico y el sistema nervioso autónomo, los factores psicológicos o el desarrollo de la placenta que regula NVE. [3] Esta patología reduce sustancialmente la calidad de vida de la mujer embarazada y requiere de intervención con antieméticos hasta que desaparezca. [10]
Antihistaminicos
De los medicamentos utilizados para el manejo de NVE algunos son antihistamínicos, estos se han utilizado siempre con precaución. Aunque, algunos autores sugieren que los antihistamínicos no tienen efectos teratógenicos. [11][12] Seto et al (1997) publicaron que los antihistamínicos utilizados durante el embarazo temprano, principalmente para tratar la enfermedad de la mañana, la seguridad no había sido demostrada y algunos estudios han reportado un aumento del riesgo teratogénico. Ellos encontraron que no existe una asociación positiva entre el uso de antihistamínicos en el primer trimestre del embarazo y malformaciones mayores. [11]
Mazzotta et al (2000) encontraron diferencias significativas en los tipos de terapias con anti-eméticos. Las fenotiazinas fueron los antieméticos más utilizados por las mujeres estadounidenses (prometazina en 36% y proclorperazina en 11%), por las mujeres canadienses los más utilizados fueron doxilamina+piridoxina en 64,8% y dimenhidrinato en 24,7%. [5] En los EE.UU., la combinación doxilamina/piridoxina (Benedectin ®) fue retirada del mercado en 1983, pero en Canadá continuó estando disponible como Diclectin ®. [8] En España hay un medicamento disponible en el mercado, con los mismos ingredientes activos que el Benedectin ®, que es recomendado durante el embarazo, [13] pero a menudo no es prescrito por la mala interpretación a cerca de su seguridad.
Aunque la combinación de doxilamine / piridoxina ha demostrado en numerosos estudios ser un medicamento seguro y eficaz en el embarazo, sólo dos de los veintiséis países de Europa utilizan este combinación de droga, uno de ellos, España. [13] Por las experiencias tan distintas de un país a otro, para tratar la NVE, han surgido trabajos como el de Koren et al (2002) o el de Niebyl JR (2010). Ellos publicaron un algoritmo basado en la seguridad para la gestión de NVE y facilitar el uso racional de los medicamentos en la terapia de NVE, tales como la vitamina B6, doxilamina, prometazina, dimenhidrinato, metoclopramida y ondasertron. [14][15] En México es común la utilización para este padecimiento de meclizina o metoclopramida.
Metoclopramida
La metoclopramida es un bloqueador del receptor de la dopamina, se utiliza comúnmente para tratar las náuseas y vómitos. [1] Es el fármaco antiemético de elección en algunos países europeos [13] y en Israel para el manejo de NVE. [16] Un estudio prospectivo encontró que la tasa de malformaciones mayores era idéntica entre el grupo control y el grupo de embarazadas que fueron expuestas a metoclopramida (1-5 por ciento). Ellos escribieron que sus datos sugieren que la administración de metoclopramida durante el primer trimestre del embarazo, probablemente, no se asocie con el aumento del riesgo de malformaciones fetales. [17] Estos resultados coinciden con otros autores. [1][16][18]
Las mujeres con NVE sufren no sólo físicamente sino también psicológicamente. Además, algunas han decidido interrumpir el embarazo en lugar de tolerar los síntomas severos. Incluso los casos menos graves de NVE puede tener efectos adversos significativos sobre la calidad de vida de una mujer, que puede afectar su trabajo, funcionamiento social, doméstico y el bienestar general. [9]
OBJETIVO
El objetivo de este reporte es describir el consumo de antieméticos durante el embarazo en España, analizar el posible riesgo teratogénico en el recién nacido de uso de doxilamine vs metoclopramida en mujeres expuestas durante el primer trimestre del embarazo y presentar estrategias para el autocuidado de la mujer embarazada.
MATERIALES Y MÉTODO
Analizamos los datos de la red del Estudio Colaborativo Español de Malformaciones Congénitas (ECEMC). Durante el periodo comprendido entre 1976 al 2008. El ECEMC es un programa de investigación clínica y epidemiológica de los defectos de nacimiento en los seres humanos.
Diseño: Es un estudio de casos y controles, La recogida de datos es de base hospitalaria e interpretación retrospectiva de la información. Definimos “caso” a todo recién nacido en cualquiera de los hospitales participantes que presente algún defecto al nacimiento (mayor y/o menor) detectable durante los primeros días de vida. Definimos “control” como el próximo niño no malformado del mismo sexo y nacido en el mismo hospital. El ECEMC tiene un “grupo periférico”, consta de 371 médicos de los hospitales que participan en el programa, que de forma altruista colaboran con el ECEMC después de haber acordado seguir su metodología común y estricta. Este grupo se responsabiliza de identificar los casos, los controles y la recolección de 312 puntos de información por cada recién nacido (la información incluye datos de la historia clínica reproductiva, planificación familia, obstétrica, y datos demográficos, ocupación materna y paterna, enfermedades de la madre agudas y crónicas, exposición de la madre durante el embarazo a alcohol, tabaco, drogas, cafeína y medicamentos). El “grupo coordinador” es un grupo multidisciplinario de expertos en dismorfología, epidemiología y teratología clínica, genética clínica, citogenética de alta resolución y molecular. También contamos con el apoyo logístico y científico de informáticos y bioestadísticos. Entre los dos grupos hay una relación constante y fluida de trabajo formando una red multicéntrica, cuyo objetivo es hacer el diagnóstico de niños con defectos de nacimiento, investigar las posibles causas y establecer medidas preventivas.
Análisis de consumo: Se consideró que los niños expuestos (casos y controles) cuya madre se expuso a fármacos antieméticos, al menos durante el primer trimestre de gestación. Para el análisis de los medicamentos antieméticos, se consideraron los expuestos a la combinación de doxilamina/piridoxina, metoclopramida y al grupo de fenotiazinas.
El periodo analizado fue desde 1977 hasta el 2008. Durante este periodo el ECEMC tuvo un total de 2 607 822 nacidos vivos consecutivos. De ellos 39 561 fueron seleccionados como casos y 38 878 como controles. 4 904 casos con síndrome de etiología conocida fueron excluidos.
Se analizó el riesgo global para defectos congénitos en hijos de mujeres tratadas con fármacos antieméticos en el primer trimestre del embarazo. En cuanto a la metodología utilizada para analizar las variables discretas, se aplicaron técnicas de inferencia estadística de homogeneidad de Chi- cuadrada con k-1 grados de libertad (donde k es el numero de clases en que se divide la variable en la que se distribuye) para medir las diferencias entre los valores en cada uno de los estratos estudiado, o entre las distribuciones de los grupos comparados se calculó la prueba de tendencia lineal (chi Cuadrada con un grado de libertad), para medir el aumento o disminución de gradientes con el aumento del valor de la variable en que se distribuye (la distribución por años y la edad materna).
Riesgo: Calculamos el odds (OR) y su IC del 95%. Los factores de confusión fueron controlados a través de un análisis de regresión logística condicionada (Stata/SE 8.0 Programa) fue aplicado por las variables de diseño. Los factores de confusión incluyeron: Edad materna, escolaridad materna, índice de masa corporal, familiares en primer grado con malformaciones congénitas, paridad, enfermedades crónicas de la madre (diabetes, cardiopatías, hipertensión, epilepsia y asma), la ingesta materna de alcohol, consumo de tabaco, drogas, cafeína, exposición a acido fólico y/o minerales, infecciones y otras enfermedades agudas, consumo de medicamentos para enfermedades del sistema respiratorio, todo durante el primer trimestre del embarazo.
Antihistamínicos: Meclozine, ciclizine prometazina. tietilperazina y dimenhidrinato.
Moduladores de la dopamina (Antagonistas de los D2): metoclopramida, proclorperazina, dixyrazine.
RESULTADOS
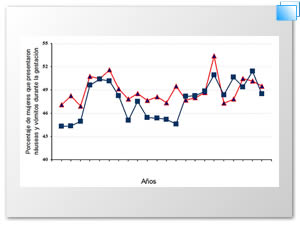
De los datos registrados en el ECEMC de 1987 al 2008, un promedio del 49% de las mujeres embarazadas ha referido presentar NVP, como se muestra en la figura 1.
Figura 1. Frecuencia de náuseas/vómitos durante el embarazo. (Periodo: 1987 – 2008).
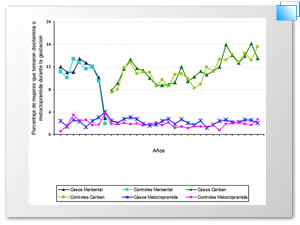
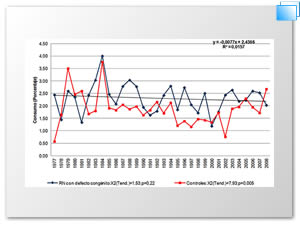
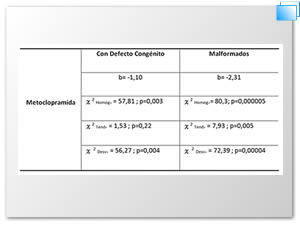
Los antieméticos que se utilizan en España son: La doxilamina/piridoxina ( Cariban®), metoclopramida y las fenotiazinas. En la figura 2, se muestra que el antiemético que más se consumió fué la doxilamina/piridoxina, en su presentación de Merbental® inicialmente y como Cariban® a partir de 1984 al 2008 (2 803 casos). El segundo antiemético que se consumió fué la metoclopramida (865 casos) como se aprecia en la figura 3, aumentando su consumo en 1984, cuando se hizo la transición del cambio de Merbental® a Cariban®. En la Tabla 1 Se presenta la tendencia de distribución del grupo de recién nacidos con defectos congénitos expuestos a metoclopramida y sus controles. La metoclopramida muestra un descenso significativo como lo indica la ji cuadrada de desviación.
Figura 2. Frecuencia en el consumo de la combinación de doxilamina + piridoxina (Merbental® y Cariban®) y metoclopramida durante el embarazo (Periodo: 1977 -2008).
Figura 3. Frecuencia del consumo de metoclopramida en mujeres embarazas. Periodo: 1977 – 2008
*RN: Recién nacidos
Tabla 1. Tendencia de distribución temporal de la metoclopramida
El tercer antiemético que se ha consumido en España son las fenotiacinas pero con pocos casos expuestos, a diferencia de los primeros dos (sólo 21 casos y 13 controles de exposición durante todo el periodo analizado) y no han demostrado tendencias significativas de incremento o descenso en su consumo. Por último el subgrupo del resto de las etanolaminas (excluida la doxilamina) con 18 casos y 9 controles).
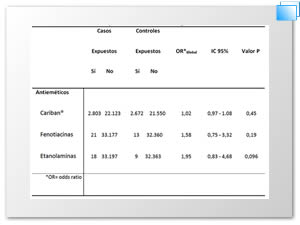
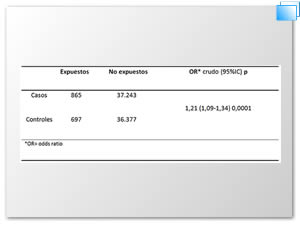
En el antiemético de mayor consumo doxilamina/piridoxina no conlleva un incremento de riesgo para defectos congénitos en la población de mujeres embarazadas españolas como se muestra en la Tabla 2 (OR= 1.02 IC 95% 0.97- 1.08; p= 0.45). La metoclopramida, el segundo antiemético de mayor consumo, si conlleva un incremento de riesgo para defectos congénitos, este incremento es pequeño pero significativo (OR= 1,21; IC 95% 1,09 – 1,34; p= 0.0001) Tabla 3. Al igual las fenotiacinas, si hubo un incremento de riesgo teratogénico (OR= 1,58; IC 95% 0,75 – 3,32; p= 0,19), y en el resto de las Etanolaminas (excepto doxilamina), (OR= 1,95; IC 95% 0,83 – 4,68; p= 0.096) Tabla 2 aunque no estadísticamente significativo.
Tabla 2. Riesgo para defectos congénitos en recién nacidos expuestos a antieméticos durante el primer trimestre de la gestación
Tabla 3. Riesgo para defectos congénitos en recién nacidos expuestos a metoclopramida durante el primer trimestre de la gestación
DISCUSIÓN Y CONCLUSIONES
Existe el 1 - 3% de probabilidad de que un niño pueda nacer con una malformación importante, incluso si la madre no tuviera exposiciones durante todo el embarazo. Este es un factor a considerar, cuando se examina la seguridad del uso de medicamentos durante el embarazo [9][19]. Hace medio siglo se reconoció a la talidomida, que había mostrado ser seguro en diversas especies de animales, podía dar lugar a graves alteraciones en el embrión y feto humano [24]. Con la retirada como antinauseoso durante la gestación de la talidomida, fue que a partir de aquí se establecieron metodología de evaluación teratológica y requerimientos regulatorios para los fármacos, por la "European Society of Study of Drug Toxicity" en 1965 y dos años después por la "World Health Organization" (Organización Mundial de la Salud).
Los ensayos controlados aleatorios en mujeres embarazadas no se realizan por razones éticas, los estudios epidemiológicos que se llevan a cabo son observacionales. Aunque estos estudios cuentan con un gran bagaje y robustez por la experiencia y casos acumulados a través del tiempo, nunca son suficiente grandes para establecer la seguridad o riesgo directamente. Por lo que la práctica de vigilancia constante de los posibles efectos teratogénicos de los medicamentos que se recetan a la embarazada, debe de ser siempre importante, como son los resultados de nuestro trabajo.
Después de la propaganda negativa alrededor de la combinación doxilamina/piridoxina en los años 80´s [8], España fue uno de los pocos países de Europa que conservó como tratamiento de primera elección para las náuseas y vómitos del embarazo (NVE) esta combinación. Nuestros resultados demuestran que doxilamina/piridoxina es el tratamiento que más es utilizado por los médicos en España para el manejo de NVE. Esta combinación parece ser no está relacionada con un riesgo teratogénico, resultados similares a la experiencia en Canadá [5][20].
Aunque hay estudios que demuestran que el uso de la combinación de doxilamina/ piridoxina en el embarazo es seguro y efectivo [21], algunas mujeres embarazadas y sus médicos son muy cuidadosos y reacios a utilizar estos fármacos en el embarazo. Causando consecuencias negativas que pueden incurrir en grandes costos económicos y emocionales. Los resultados de este trabajo pueden ayudar al clínico a agilizar la toma de decisión al tratar los casos de NVE de forma oportuna, mejorar los autocuidados de la mujer embarazada y no esperar las complicaciones. Los medicamentos antieméticos, tales como los antihistamínicos H1 o la metoclopramida, han estado disponibles por 40 años para ayudar a las mujeres embarazadas y tratar esta enfermedad. Muchos medicamentos no hay sospecha de incrementar la teratogenicidad y deben de estar disponibles en la mayor parte del mundo para ayudar a las mujeres embarazadas para tratar o manejar su NVE, por lo tanto, esta condición no se debe dejar sin tratar [9].
El impacto que tuvo el identificar a la talidomida como agente causal de la epidemia de defectos congénitos en la década de los 60 [24] llevó al colectivo médico y a la población en general que se hicieran muy reacios a prescribir o consumir cualquier tipo de medicamento durante la gestación. Aunque las náuseas y vómitos del embarazo sea un síndrome causado por la compleja interacción de factores genéticos y ambientales ocurridos durante el periodo de la organogénesis [22], Este síndrome necesita ser tratado de forma eficaz durante este tiempo que es cuando el riesgo de malformaciones en el embrión es alto.
En los estudios caso-control, como es el desarrollado en nuestro trabajo, cuando existe un número de casos suficiente se selecciona un control por caso. Se podría aumentar la potencia estadística del estudio si se seleccionara más de un control por cada caso, sin embargo esto no pone en duda los resultados efectivamente encontrados en el presente estudio. El seleccionar un número mínimo de controles por caso fue que de esta forma los controles eran lo más parecido en cuanto a compartir atributos comunes con los casos como edad, sexo, residencia o lugar geográfico de vida común o grupo étnico.
En los estudios caso-control, el grupo de casos debe incluir todos los casos o una muestra representativa que aparecen en una población definida, en nuestro estudio son los recién nacidos con algún defecto congénito. Consideramos que si en la base de datos del ECEMC recogió el 21.55% del total de nacimientos en España [25], este es un porcentaje representativo de la población de recién nacidos españoles y por lo tanto la información aquí presentada no tiene sesgo de selección relevante.
Los manuales de recogida de la información del ECEMC indican que cuando se identifica un caso, la información se le pregunta a la madre dentro de los primeros 3 días de nacido del caso, esto obliga a que la información sobre la historia de exposiciones pasadas sea de forma retrospectiva. No se obtiene de personas próximas (familiares o amigos) que podrían sesgar la información recopilada. Consideramos que en nuestro estudio, no es probable el sesgo del entrevistador, ya que los médicos que recaban la información, de tanto casos como controles, en los hospitales integrantes del Grupo Periférico, son diferentes a los que integran la información en el Grupo Central del ECEMC (quien diseña las investigaciones), esto evita que los médicos entrevistadores puedan preguntar con más detalle e insistencia a los casos que a los controles.
Estamos conscientes que el sesgo puede ocurrir en todas las modalidades de diseños de investigación epidemiológica, y en esta tesis no podemos negar que puedan existir otros sesgos de extraordinaria complejidad que pudimos pasar inadvertidos.
Una de las ventajas de la base de datos del ECEMC es que tiene un gran grado de información, gracias a que desde su fundación hace 35 años se puede contar con un gran número de casos y sobre todo cuando se trata de investigar sobre la exposición de AH1 en las mujeres gestantes, estado fisiológico de la mujer en la que tiende a disminuir la cantidad de fármacos a prescribir. Los estudios caso-control como el del ECEMC son muy eficientes en tiempo, coste y posibilidad de estudiar varios factores de forma simultánea, por lo que se pude realizar en México uno similar para el seguimiento de las mujeres que toman fármacos durante su gestación. En España el antihistamínico antiemético de mayor consumo es la doxilamina (en su presentación doxilamina + piridoxina) el cual en el periodo estudiado de este trabajo, no se observó un incremento de riesgo teratogénico, por lo tanto, se mantiene como de elección para tratar la NVE, en atención primaria. Dejando a la metoclopramida como segunda opción, sólo en caso de que la combinación doxilamia + piridoxina fracase o en atención hospitalaria. Debemos tratar la NVE y mejorar el autocuidado de la mujer embarazada.
Tabla 4. Pautas para la selección racional de Antieméticos durante la gestación
Bibliografía
[1]Bercovitch M, Mazzotta P, Greenberg R, Elbirt D, Addis A, Schuller-Faccini L, et al. Metoclopramide for nausea and vomiting of pregnancy: A prospective multicenter international study. Am J Perinatol. 2002; 19(6):311-316.
[2]Tyack AL. Vomiting in pregnancy. Current Obstetrics & Gynaecology. 1991; 1(2): 93-96.
[3]Huxley RR. Nausea and vomiting in early pregnancy: its role in placental development. Obstet Gynecol. 2000;95:779-792
[4]Lacasse A, Rey E, Ferreira E, Morin C, Bérard A. Epidemiology of nausea and vomiting of pregnancy: prevalence, severity, determinants, and the importance of race/ethnicity. BMC Pregnancy and childbirth. 2009;9:26
[5]Mazzotta P, Maltepe C, Navioz Y, Magee LA, Koren G. Attitudes, management and consequences of nausea and vomiting of pregnancy in the United States and Canada. International Journal of Gynecology & Obstetrics. 2000; 70: 359-365.
[6]Klebanoff MA, Koslowe PA, Kaslow R, Rhoads GG. Epidemiology of vomiting in early pregnancy. Obstet Gynecol. 1985; 66:612-616.
[7]Gazmararian JA, Petersen R, Jamieson DJ, Schild L, Adms MM, Deshpande AD, Franks AL. Hospitalization during pregnancy among managed care enrollees. Obstet Gynecol. 2002; 100(1):94-100.
[8]Ornstein M, Einarson A, Koren G. Bendectin/Dicletin for morning sickness; a Canadian follow-up of an American tragedy. Report Toxicol. 1995; 9:1-6.
[9]Gill SK, Einarson A. The safety of drugs for treatment of nausea and vomiting of pregnancy. Expert opinion on Drug Safety. 2007; 6 (6): 685-694.
[10]Asker C, Norstedt B, Källén B. Use of antiemetic drugs during pregnancy in Sweden. Eur J Clin Pharmacol. 2005; 61:899-906.
[11]Seto A, Einarson T, Koren G. Pregnancy outcome following first trimester exposure to antihistamines: meta-analysis. Am J Perinatol. 1997; 14:119-124.
[12]Källén B. Use of antihistamines drugs in early pregnancy and delivery outcome. J Mat Fetal Neonat Med. 2002; 11:146-152.
[13]Einarson A, Koren G, Bergman U. Nausea and vomiting in pregnancy: a comparative European study. Eur J Obstet Gynecol Reprod Biol. 1998; 76: 1-3.
[14]Koren G. Levicheck Z. The teratogenicity of drugs for nausea and vomiting of pregnancy: Perceived versus true risk. Am J Obstet Gynecol. 2002; 186 (5):248-52.
[15]Niebyl JR. Nausea and vomiting in pregnancy. N Engl J Med. 2010; 363 (16):1544-50.
[16]Matok I, Gorodischer R, Koren G, Sheiner E. Wiznitzer A, Levy A. The safety of metoclopramide use in the first trimester of pregnancy. N Engl J Med. 2009; 360 (24): 2528-35.
[17]Bercovitch M, Elbirt D, Addis A, Schuler-Faccini L, Ornoy A. Fetal effects of metoclopramide therapy for nausea and vomiting of pregnancy. N Engl J Med. 2000; 343:455-6.
[18]Sorensen HT, Nielsen GL, Christensen K, Tage-Jensen U, Ekbom A, Baron J. Bith outcome following maternal use of metoclopramide. Br J Clin Pharmacol. 2000; 49:264-268.
[19]Nguyen P, Einarson A. Managing nausea and vomiting of pregnancy with pharmacological and nonpharmacological treatments. Fut Med. 2006; 2:753-760.
[20]Chandra K, Magee L, Einarson A, Koren G. Nausea and vomiting in pregnancy: results of a survery that identified interventions used by women to alleviate their symptoms. J psycho. Obstet. Gynaecol. 2003; 24:71-75.
[21]Magee LA, Mazzotta P, Koren G. Evidence-bases view of safety and affectiveness of pharmacologic therapy for nausea and vomiting of pregnancy (NVP). Am J Obstet Gynecol. 2002; 186(5): Suppl: S256-S261.
[22]Goodwing TM. Nausea and vomiting of pregnancy: An obstetric syndrome. Am J Obstet Gynecol. 2002; 186 (5):S184-S189.
[23]Lacasse A, Rey E, Ferreira E, Morin C, Bérard A. Nausea and vomiting of pregnancy: what about quality of life? BJOG. 2008; 115(12):1484-1493.
[24]Lenz W. A short history of Thalidomide embryopathy. Teratology.1988; 38: 2003-2015.
[25]E Bermejo, L Cuevas, Grupo periférico del ECEMC, Martínez-Frías ML. Vigilancia epidemiológica de anomalías congénitas en España. Análisis de datos de registro del ECEMC en el periodo 1980-2008. Bol ECEMC: Rev Dismor Epidemiol 2009; V, 8:64-91
[1] Profesor Investigador de la Universidad Autónoma del Estado de Hidalgo
[a] Profesor del Área Académica de Enfermería, Instituto de Ciencias de la Salud, Universidad Autónoma del Estado de Hidalgo, México
[b] Estudio Colaborativo Español de Malformaciones Congénitas (ECEMC), Centro de Investigación de Anomalías Congénitas (CIAC), Instituto de Salud Carlos III, Ministerio de Sanidad y Consumo, Madrid, España.
[c] CIBER de Enfermedades Raras (CIBERER). Ministerio de Ciencia e Inovación, Madrid, España.
[d] Departamento de Farmacología, Facultad de Medicina, Universidad Complutense de Madrid, España